据相关行业调研数据,截至日前,新型冠状病毒核酸检测试剂盒研发企业已超过120家,底层技术应用原理大都是以基因扩增技术打底。而这背后所折射出来的,其实就是分子诊断技术大家族。
未来3-5年IVD行业最具发展潜力的产品线是什么?答案无疑是分子诊断。
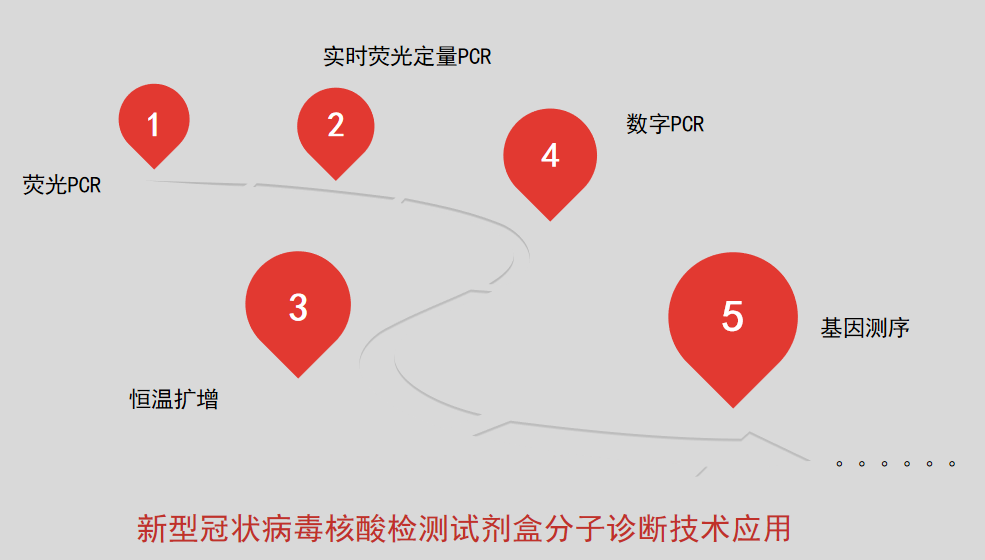
新型冠状病毒核酸检测试剂研发—分子诊断技术应用
总的来讲,分子诊断技术是指以DNA和RNA为诊断材料,用分子生物学技术通过检测基因的存在、缺陷或表达异常,从而对人体状态和疾病作出诊断的技术。其基本原理是检测DNA或RNA的结构是否变化、量的多少及表达功能是否异常,以确定受检者有无基因水平的异常变化,对疾病的预防、预测、诊断、治疗和预后具有重要意义。
按照技术原理,可以将上市分子诊断技术大致划分为PCR技术、分子杂交、基因测序、核酸质谱、生物芯片5大类。

分子诊断技术大家族
截止2020年3月,分子诊断产品获批数量超1200项。从目前市场分子诊断产品来看,基于核酸诊断技术的产品仍占主要。从各类技术类别来看,PCR技术由于壁垒相对较低,国产化程度高,国内企业布局相对较早,因此基于PCR技术的分子诊断产品占总产品量的70%以上。
从此次新型冠状病毒肺炎产品注册就可以看出,PCR技术发展已经很成熟了。下面我们就来逐一解剖一下分子诊断技术这个大家庭!
01
基因扩增技术(PCR技术)
在1983年,美国人Mullis发明了聚合酶链反应技术(polymerase chain reaction, PCR),这一技术将DNA的变性原理以及复性原理加以利用,采用适温延伸、高温变性以及低温复性,让核酸片段实现了体外扩增,可将极微量的目标DNA特异地扩增上百万倍,从而提高对DNA分子的分析和检测,因为PCR有着很高的灵敏度以及特异性,而且简便快速,所以这种技术已经成为目前临床基因扩增实验室接受程度最高的技术。同时,PCR技术又可以分为定量PCR和常规PCR,定量PCR分为实时荧光定量PCR(RT-PCR)和数字PCR。

PCR技术大致分类
但伴随着PCR技术的迅猛发展,有关这项技术的质量管理问题也日益突出,如何消除各类生物学变量所引起的检测变异,减少或抑制实验操作与方法学中的各种干扰因素是PCR技术面临的难题。比如此次新型冠状病毒核酸检测假阴性问题,就是技术面临的一些现实问题。
02
基因测序技术
基因测序是直接获得核酸序列信息的唯一技术手段,是分子诊断技术的一项重要分支。虽然分子杂交、分子构象变异或定量PCR技术在近几年已得到了长足的发展,但其对于核酸的鉴定都仅仅停留在间接推断的假设上,因此对基于特定基因序列检测的分子诊断,核酸测序仍是技术上的金标准。
图片来源:网络
第1代测序
1975年Sanger与Coulson发表了使用加减法进行DNA序列测定的方法,随后Maxam在1977年提出了化学修饰降解法的模型,为核酸测序时代的来临拉开了序幕。经典的Sanger测序技术,被称作是测序界的金标准。随着高通量测序技术应用拓展,基因测序技术将不断升级,也将进一步提高占比,成为未来肿瘤检测的主要技术。目前测序市场主流为NGS测序平台。
第二代测序
NGS高通量测序技术又称第二代的测序技术,就是对几百万到数十亿的DNA分子一次性实现并行测序。可对一个物种的全部转录组和基因组进行深入、细致地分析。在基因组水平上对未知序列的物种进行从头测序,获得该物种的基因序列,为后续的进一步研究奠定基础;进行参考序列物种的全基因组测序,并在全基因组这一水平之上进行突变位点的检测,发现个体差异的分子变化。
第三代测序
第三代测序技术的核心理念是以单分子为目标的边合成边测序,单分子测序平台给测序技术带来新思路,部分已经开始商业化推广,但尚未达到NGS的规模。
相比二代测序,第三代测序技术在临床上的应用有明显优势:第三代测序技术不需要PCR扩增,可直接对单个分子进行测序;样品制备简单,测序成本进一步降低;可直接读取RNA的序列和包括甲基化在内的DNA修饰。这些优势可以大大改善临床基因测序的成本、速度和质量,但单分子测序有通量限制,所以并不适合独立做全基因组测序,更适于针对有限的、个性化的、目标性的应用。
03
分子杂交技术
分子杂交就是指两条有着同源序列的核酸单链,通过碱基互补配对这一原则相结合,进而形成双链的这一过程,它能够通过已知序列的基因探针对目标序列加以捕获和检测。
进行杂交的双方分别是探针以及有待探测的核酸,有待检测的对象可以选择基因组的DNA,也可以选择细胞总DNA,可以对其进行提纯,也可以对其进行细胞之内的杂交,也就是细胞原位杂交。必须对探针进行标记,这样才可以进行示踪以及检测。

图片来源:网络
同位素是最为普遍应用的探针标记物,多使用类化合物地高辛配基(digoxigenin,DIG)标记。核酸分子杂交因具有高灵敏度和高特异性,在分子生物学领域中已广泛地使用于克隆基因的筛选、基因组中特定基因序列的定性、定量检测等方面因为核酸分子杂交的灵敏度以及特异性都很高,因此这一技术已经在克隆基因筛选以及基因组之中待测的基因序列定性、定量检测之中得到了广泛的应用。
04
核酸质谱技术
目前核酸分析所使用的质谱电离技术主要还是采用 ESI 和MALDI。简单来讲,两种电离技术都是软电离,ESI 检测的特点是生物大分子带多个电荷,质荷比范围基本在2000 Da 以下区间,从而能检测几万乃至更大的生物分子;而MALDI 常得到单电荷峰,与飞行时间(TOF)分析器搭配,检测范围可以到几十万道尔顿。
质谱技术相比于其他检测技术具有快速、准确、灵敏度高、高通量等优点,近年来在核酸的高级结构鉴定、寡核苷酸与小分子的相互作用、DNA 损伤与修饰等领域有着广泛的应用。
由于生物样品的复杂性,质谱技术还面临着一些挑战和困难。但生物质谱技术是科学研究的有力工具,随着临床实验室对质谱的了解和应用不断的加深,未来该检测平台或可成为规范实验室不可或缺的标准装备。
05
生物芯片技术
生物芯片技术在最近的一些年里才得到了发展,这种分析与检测的技术将分子生物学以及微电子技术之间进行有效结合。因此,这种技术又被称作基因芯片技术或者是DNA芯片技术。在当今,这一技术在免疫反应以及受体结合等的这些非核酸领域之中得到了广泛的扩展,出现了组织芯片、细胞芯片、免疫芯片以及蛋白质芯片等,所以又将官这种技术改称作生物芯片技术。
生物芯片技术是通过微加工和微电子技术,在固相基质表面集成密集排列的分子微阵列,以实现对核酸、细胞、蛋白质、组织以及其他生物分子进行高效、准确的检测。生物芯片技术的本质特征是将生命科学研究中的样品制备、生化反应以及检测分析等过程实现连续化、集成化及微型化。

图片来源:网络
微阵列芯片
也就是常说的基因芯片,又称DNA微阵列(DNA micro-array)、SNP芯片,是把大量已知序列探针集成在同一个基片(如玻片、膜)上,经过标记的若干靶核苷酸序列与芯片特定位点上的探针杂交,通过检测杂交信号,对生物细胞或组织中大量的基因信息进行分析。
与传统的染色体核型分析技术相比具有更高的分辨率,可识别Kb级别以上的染色体细微失衡。基因芯片目前已成为国内外临床遗传学诊断的一项常规的技术,在遗传病检测、疾病筛查、疾病分型、病原体检测、个性化用药等方面均呈现出广阔的应用前景。全球知名的芯片公司有 Illumina、Affymetrix(于2016年被赛默飞收购)、安捷伦等。
微流控芯片
微流控芯片( microfluidic chip) 由微米级流体的管道、反应器等元件构成,与宏观尺寸的分析装置相比,其结构极大地增加了流体环境的面积/体积比,以最大限度利用液体与物体表面有关的包括层流效应、毛细效应、快速热传导和扩散效应在内的特殊性能,从而在一张芯片上完成样品进样、预处理、分子生物学反应、检测等系列实验过程。目前使用微流控芯片进行指导用药的多基因位点平行检测是主要临床应用领域。
06
总结:分子诊断市场未来可期!
分子诊断技术的应用不仅深化对疾病发病机制分子生物学的基础研究,而且不断扩大了分子诊断疾病的病种,随着人类基因组计划的完成和蛋白质组计划的启动,分子诊断方法将极大地推动现代检验医学的迅速发展,并通过这些基本技术的衍生、联合产生新的分析方法,从而提高分子诊断的特异性、敏感性和准确性,为临床医学诊断和治疗提供更准确的数据和信息。
本文来源:IVD从业者网,先达基因(www.gendx.cn),本文转自搜狐网,不代表深蓝医疗观点,若有侵权,请及时联系删除。



